公開
本章では、各放射性同位体ごとの特徴や半減期などの値についてまとめておきます。
数値の引用は、半減期と放射線のエネルギーが(1)、
実効線量係数が(2)、
濃度限界(法律による排出規制)が(3)です。
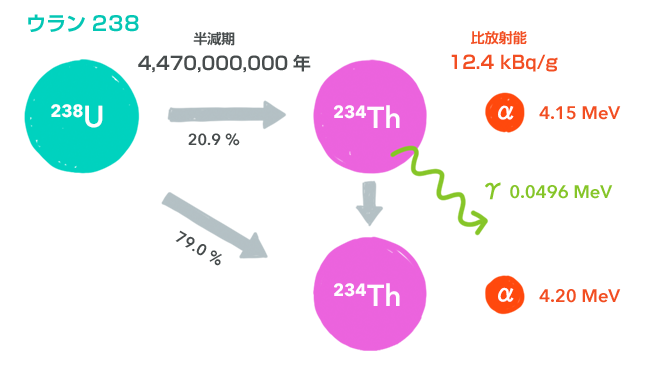
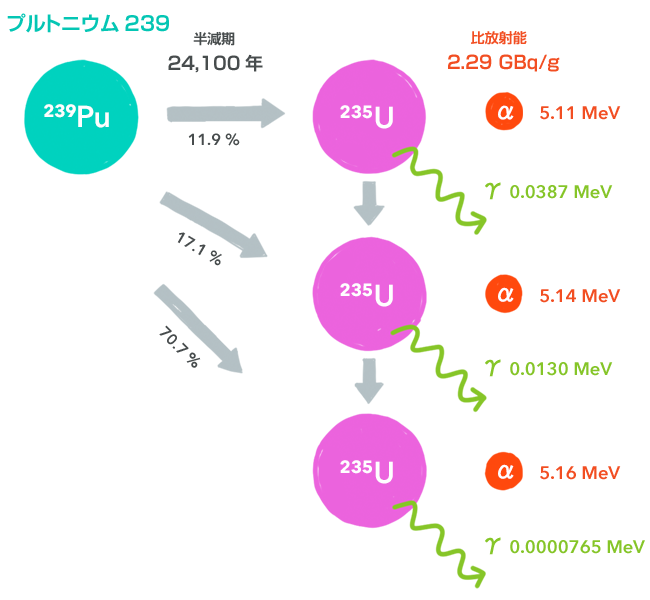
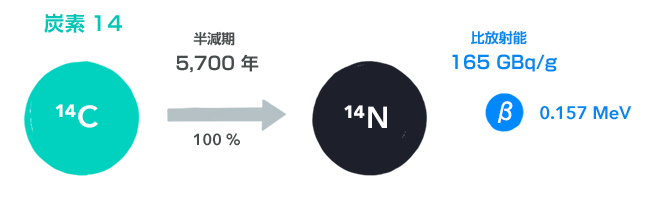
各節に載せた図は、崩壊のようすをイラスト化したものです(4)。放射性同位体が崩壊してどの同位体に変化し、どんな放射線を出すのか、を描いています。
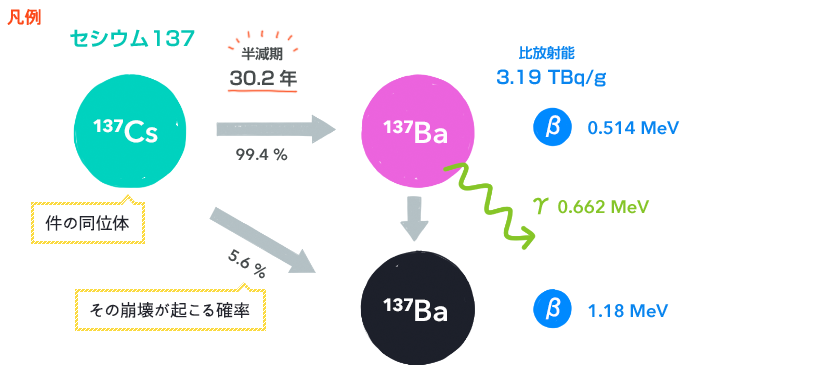
矢印の上の数値が半減期で、矢印の下の数値がその崩壊が起こる確率です。崩壊のしかたは、同位体によってはとても多い場合がありますので、おもなものだけを描いてあります。
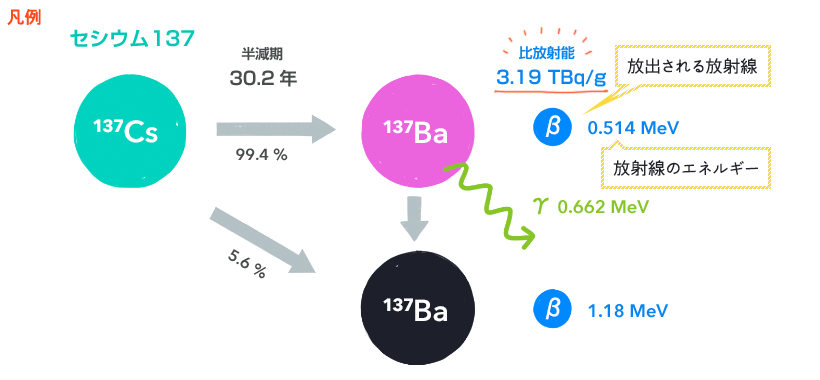
放射線の上の数値が比放射能です。放射線の右の数値が放射線のエネルギーです。
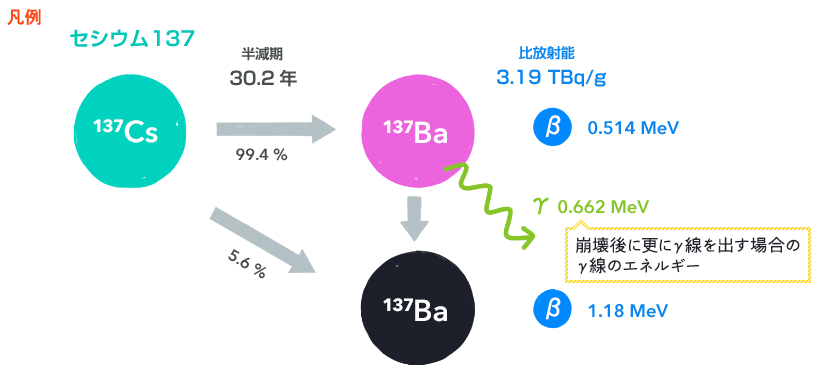
崩壊後の同位体から「γ」とある矢印が延びているのは、その状態では不安定で、安定するためにγ線を放出することを意味しています。
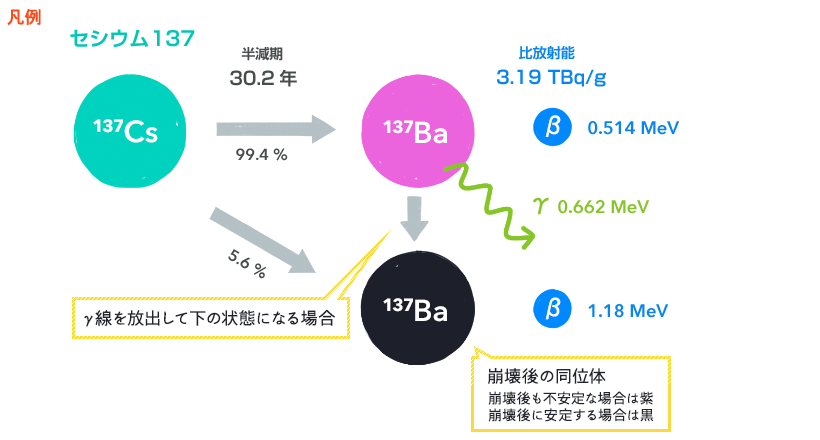
γ線を放出すると下の状態になる場合には、矢印でつないであります。安定した(放射線を出さない)状態になった同位体は、黒で描いてあります。また、ニュートリノは省略してあります。
α線を出す放射性同位体
放射線は、不安定な原子核が崩壊して安定な状態へと近づいていく際に放出されるものでした。その放射線の放出の仕方は第2章でお話ししたとおりですが、α崩壊やβ崩壊のときには、原子核が別のものに変わってしまっています。崩壊前の原子核を親核種、崩壊後の原子核を娘核種と呼びます。娘の段階で安定しないと、その娘は自分が親となって崩壊し、さらにその娘を産みます。このような親娘の関係を系統図にすると、放射性同位体の「家系図」ができあがります。これを「崩壊系列」と呼んでいます。
これも第2章でお話ししたとおり、α崩壊の場合、原子番号は2つ、質量数は4つ、それぞれ減っていきます。ひとつの家系では、質量数は4ずつ飛び飛びで減っていくことになるわけです。そのため、これらの家系には、質量数が、「4の倍数」の家系、「4の倍数+1」の家系、「4の倍数+2」の家系、「4の倍数+3」の家系、の4つがあり、それぞれ、「トリウム系列」、「ネプツニウム系列」、「ウラン系列」、「アクチニウム系列」と呼ばれています。
本章では、まず、もっとも有名な家系である「ウラン系列」の一族についてみていきましょう。
ウラン238(238U)
「ウラン系列」という名前がついているのは、その家系の祖先がウラン(238)だからです。この家系のすべての同位体の母、ウラン238についてみてみましょう。
| 実効線量係数 | 吸入 | 成人 | 8.0x10-6 Sv/Bq |
|---|---|---|---|
| 幼児 | 2.5x10-5 Sv/Bq | ||
| 摂取 | 成人 | 4.5x10-8 Sv/Bq | |
| 幼児 | 1.2x10-7 Sv/Bq | ||
| 排気中濃度限界(六弗化ウラン等) | 3x10-7 Bq/cc | ||
| 排気中濃度限界(二酸化ウラン等) | 2x10-8 Bq/cc | ||
| 排水中濃度限界 | 2x10-2 Bq/cc | ||
実効線量係数で、吸入が摂取より2けたほど大きくなっているのは、α線を放出する放射性同位体の特徴です。粉塵を吸い込むことで、肺の中に留まり、肺組織を攻撃します。肺は行き止まりになっていますから、そこから出て行きにくいのです。
ウラン238がすべての母である理由は、地球上に豊富に存在しているからです。こういった大きな質量数をもつ同位体は、恒星(太陽系でいえば、太陽のひとつ前の世代の恒星)が死ぬときの反応(超新星など)によってつくられます。そのときにはあらゆる種類の同位体がつくられるのですが、短い寿命のものはどんどん崩壊してなくなっていきます。それらが集まって惑星をつくり、それから50億年たった今でも豊富に残っているということは、それだけ寿命が長いことを意味しています。
たとえば地球上のウランの同位体存在比は、ウラン238が99.3%、ウラン235が0.7%ですが、そのような比率となったのは、それぞれ、45億年と7億年という半減期の違いによるものです。半減期が短いウラン235のほうが早く壊れてしまい、現在まで残った数が少なくなってしまった、ということです。ウラン238がすべての母となって放射性同位体をつくり続けていられるのは、この地球自体と同じくらいに長い寿命のおかげです。45億年という半減期は、これから本章で紹介するほかの放射性同位体と比べて、けた違いに長いと感じることでしょう。
このような長寿命の同位体が祖先であるため、ウラン238の子孫たちは安定した供給元をもつことになります。そのため、自身の半減期が短いものでも、常にウラン238からつくられ続け、一定の量が地球上に存在します。
ウラン238は花崗岩に多く含まれ、したがって、その娘たち(放射性同位体)が多く含まれるのも花崗岩ということになります。第6章でお話ししたとおりです。他の鉱物資源同様、地上には偏って存在しています。ウランの産出量では、カザフスタン、カナダ、オーストラリアの順に多く(5)、埋蔵量では、オーストラリア、カザフスタン、ロシアの順です(6)。ただし、埋蔵量が他国に充分に把握されていない北朝鮮は、相当量の埋蔵量を有すると考えられており、一説によると、世界最多、それも、他のすべての国の埋蔵量を合わせたものぐらいあるとさえ言われています。
日本でも岡山県の人形峠で試掘したことがありましたが、結局はウランを輸入する方針となったために、現在では採掘は行われていません(7)。
ウラン235は天然資源として利用できるほとんど唯一の核分裂物質であるため、核兵器の製造や原子力産業には欠かせないものですが、ウラン238は、おもに、そのウラン235を抽出するために一緒に採掘されます。濃縮によってウラン235を抽出した後のウラン238は、ではまったくの廃棄物扱いなのかというと、ちゃんと利用方法があります。
ひとつは、やはり原子力産業での利用で、中性子を吸収させることでプルトニウム239を製造します。詳しくはプルトニウム239のところに書いておきます。
ふたつめは、核兵器への利用です。ウラン238は、一般的な原子炉内の中性子のエネルギーでは核分裂を起こしませんが、核融合反応で発生するような高速の中性子を吸収すると、核分裂を起こします。そのため、核兵器に組み込むことで、その核出力の一端を担います。このあたりの話は本サイトの範囲を超えますので、詳しくは拙著『核兵器』(明幸堂)をごらんください。
みっつめは、放射性同位体としての利用ではなく、その物性を利用した方法です。
現代の戦車の砲弾は、従来の砲弾とはまったく異なるメカニズムで装甲を破るため、その弾芯(侵徹体)は特殊な形状をしています。ここでは詳しくは話しませんが、その材質は、比重が大きいことが重視されます。そこで、砲弾のように使い捨てしてもよいくらいの価格で手に入るもので比重が最大級の材質ということで、ウラン合金が使われているのです。みなさんも、「劣化ウラン弾」という言葉を聞いたことがあるかもしれません。「劣化」の意味するところは、天然ウランの中からウラン235を抽出し、ウラン235の濃度が少なくなった、ということなのであって、原子力産業的には「劣化」でも、物性的に「劣化」しているわけではありません。ですので、僕は、砲弾として利用しているものを「劣化ウラン」と呼ぶのは適切ではないと思っています。
ウラン238は半減期がきわめて長い、つまり比放射能が低いのですが、それでも、砲弾のように相手に撃ち込んで使い捨てるものに放射性物質を用いることは、倫理的に問題があります。特に、現代の戦車砲弾は、大雑把に言うと、弾芯が装甲を削り取りながら自らも削れていくことで貫徹しますので、使用後は塊ではなく細かく分かれてしまいます。α線を放出する放射性同位体は、内部被曝が問題となることはお話ししたとおりですから、これは問題です。
そのため、ほとんどの国では戦車砲弾にウラン合金の代わりにタングステン合金を用いています。ただ、貫徹力ではウラン合金のほうが大きく、しかもウラン合金は貫徹した後の焼夷効果もあり、砲弾としては理想的であるために、ロシアやアメリカはウラン合金製の砲弾を使っています。国内戦を前提とするドイツや日本がタングステン合金弾を使用し、外国でしか戦わない、つまり国内ではなく他国に砲弾を捨ててくることが前提のアメリカがウラン合金弾を使用していることは、とてもわかりやすいことだと思います。ただ、使い捨てではない用途として、アメリカでは戦車の装甲にもウラン合金を使用しています。
ところでウランという名前は、日本人であれば、「鉄腕アトム」に登場した、アトムの妹であるウランちゃんを思い浮かべる人も多いかも知れません。語源としては、ローマ神話における天空の神Uranus(ギリシア神話のΟυρανόςに相当)に由来します。
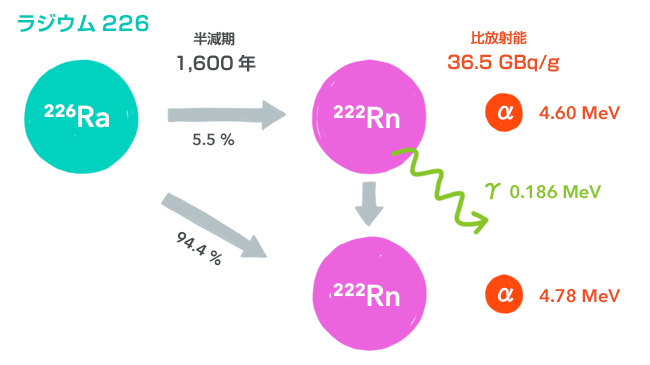
ラジウム226(226Ra)
ウラン238がα崩壊してトリウム234となり、それが2回のβ崩壊を経てウラン234となり、そこから2回のα崩壊を経てラジウム226となります。
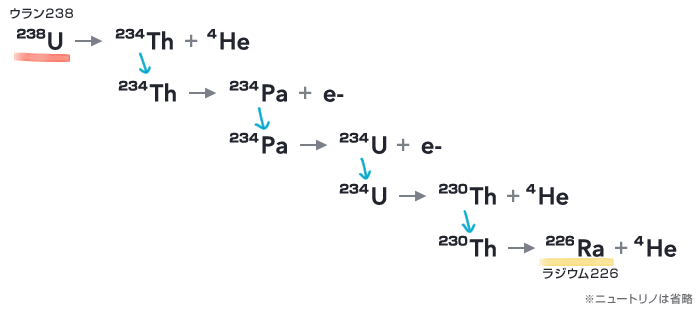
238U → 234Th + 4He
234Th → 234Pa + e-
234Pa → 234U + e-
234U → 230Th + 4He
230Th → 226Ra + 4He
(ニュートリノは省略)
| 実効線量係数 | 吸入 | 成人 | 9.5x10-6 Sv/Bq |
|---|---|---|---|
| 幼児 | 2.9x10-5 Sv/Bq | ||
| 摂取 | 成人 | 2.8x10-7 Sv/Bq | |
| 幼児 | 9.6x10-7 Sv/Bq | ||
| 排気中濃度限界 | 4x10-8 Bq/cc | ||
| 排水中濃度限界 | 2x10-3 Bq/cc | ||
ラジウムは、ある意味、放射性同位体の象徴的存在です。Radiumという名前自体が、放射線(radiation)のラテン語radiusから由来していることもそれを如実に表わしています。また、放射能の単位は現在ではBqですが、大昔はCi(キュリー)という単位が使われており、このCiは、ラジウムの比放射能をもとにつくられたものです。それくらい、初期の放射線の研究において中心的役割を果たしたものです。
そして、Ciという単位にも使われているように、ラジウムの研究でもっとも有名なのは、その発見者でもあるマリア・スクウォドフスカ・キュリーでしょう。放射能と放射性同位体の概念を考え出したのも彼女です。ノーベル物理学賞と化学賞の両方を受賞した唯一の学者で、フランスを除くあらゆるヨーロッパの国々から100を超える称号を得ました。が、肝心の本国フランスからは、女性であることと外国出身であることを理由に冷遇され、これだけ偉大な学者であるにもかかわらず、生活は苦しかったそうです。それでもフランスのために全力で貢献し、第1次世界大戦では、自ら資金集めを行ってX線撮影設備を調達し、戦傷者の治療に計り知れない貢献をしました。戦闘によって体内に喰い込んだ破片や弾丸を発見するのに、X線撮影は絶大な威力を発揮したからです。学者が、自らの専門知識を活用して積極的に社会に貢献した、きわめて偉大なる先例です。
ラジウムの同位体はたくさんありますが、1日を超える半減期を持つものは5つ、そのうち1年を超える半減期を持つものは2つで、ラジウム226は最長の1600年の半減期を持ちます。
ラジウム226といえば、2011年に、世田谷区の民家の床下から、ラジウム226入りの容器が発見された事件を憶えておられる方がいるかもしれません。これは、福島第一原子力発電所事故後に、道路などの一般区域の放射線量を測定していたときに、偶然発見されたものです。なぜ普通の民家に放射性物質が…と思われたかも知れませんが、ラジウム226は、かつては、夜光塗料として時計の文字盤などに使われていたのです。アメリカの時計工場でこの作業をしていた人たちが内部被曝による健康被害で訴訟を起こしたこともあります。この民家に数十年住んでおられた方が知らなかった、つまりその方が引っ越されるよりも前、数十年以上前からあったということですから、相当古いもので、放射性物質の管理が今ほど厳しくなかった時代のものだったのでしょう。
ところで、ここまでよくこのサイトを読んで下さっている方は、α線を放出するラジウム226が床下にあったにもかかわらず、なぜ検知されたのか、不思議に思われるかも知れません。α線の飛程では、容器の外に出ることもできませんからね。それは、さきほどの崩壊の図をよくごらんいただけるとわかります。安定するまでに、α線以外にも、γ線も放出しているからです。このγ線が検出され、発見につながったのです。第9章で、ラジウムを管に入れて膣内に挿入する子宮癌治療の話をしましたが、そこで「α線やβ線を管の壁で遮蔽し、γ線だけを人体に照射するため」と書いたとおり、治療に使うのはこの余分に出てくるγ線なのです。
ラジウム226自体は、他に様々な放射性同位体が利用されるようになった現代ではほとんど利用されることがありませんが、ラドン222の直接の親ですので、そういう意味では重要です。
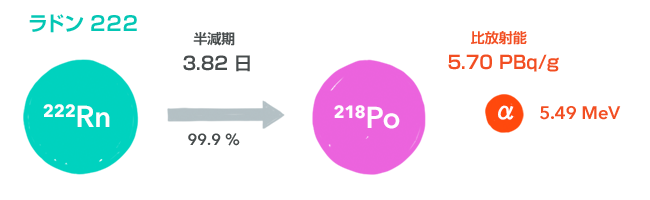
ラドン222(222Rn)
ラジウム226がα崩壊してラドン222となります。

226Ra → 222Rn + 4He
| 排気中濃度限界 | 2x10-5 Bq/cc | ||
|---|---|---|---|
ラドンのような希ガスには、実効線量係数はありません。体内に取り込まれるというよりも、たとえば肺の中に滞留した空気に含まれるラドンが、そこから肺組織を攻撃するからです。
ラドンも、放射性同位体としては重要な立場にあります。Radonという名前も、ラジウムと同じく、radiusからとられています。発見当初は、ラドン219とラドン220はラドン222と別の元素だと考えられていたために、ラドン219はアクチノン、ラドン220はトロン、と呼ばれていました。
ラドンの問題は、第6章でお話ししたとおり、これが常温で気体だということです。ウランから始まって、その中間段階であるトリウムもプロトアクチニウムもラジウムも固体で、鉱石の中に閉じ込められていますが、ラドンになったとたん、気体となって、空気中に飛び出すのです。内部被曝の観点からは、固体は気をつければ摂取を抑えることが可能ですが、気体はかんたんに吸入してしまいます。第6章で紹介した年間被曝量の世界平均の実に半分がラドンの吸入によるものであるのも、誰もが常に吸っている空気の中に、ラドンが含まれているからです。ラドンは無色無臭ですので、五感でその存在を知ることはできません。
気体であるがゆえに吸入を防ぐことがむずかしいラドンも、気体であるがゆえに減らすことはかんたんです。換気に気を配ればよいのです。岩石、とくに花崗岩が含まれる洞窟や、石づくりの建造物、そういったところではラドンが出ている可能性が高いですから、空気が澱まぬように、換気をよくすることが重要です。ラドンの比重は空気よりはるかに大きいので、室内でも下のほうに溜まりやすいですから、その点も考慮して換気するとよいでしょう。
第6章で、ラドンによる被曝は、喫煙の次に多くの肺癌を引き起こしている(8)、という話をしましたが、ひとつ具体的な研究結果を紹介しておきますと、ラドン濃度が150Bq/m3になると、肺癌のリスクが24%上がるそうです(9)。「人工放射線が問題なのであって、自然放射線は問題がない」などということがまったく荒唐無稽であることがわかるでしょう。
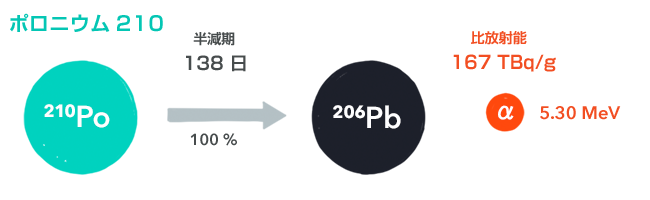
ポロニウム210(210Po)
ラドン222が2回α崩壊して鉛214になり、それが2回β崩壊してポロニウム214になります。さらにそれがα崩壊して鉛210になったあと、2回β崩壊してポロニウム210となります。
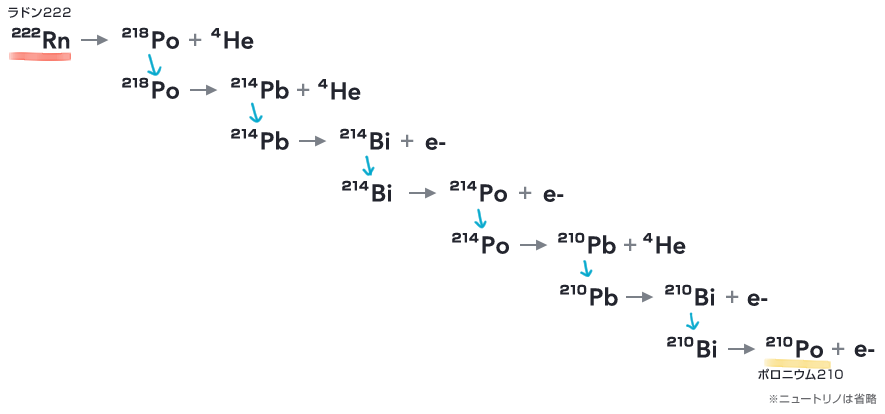
222Rn → 218Po + 4He 218Po → 214Pb + 4He 214Pb → 214Bi + e- 214Bi → 214Po + e- 214Po → 210Pb + 4He 210Pb → 210Bi + e- 210Bi → 210Po + e- (ニュートリノは省略)
| 実効線量係数 | 吸入 | 成人 | 4.3x10-6 Sv/Bq |
|---|---|---|---|
| 幼児 | 1.4x10-5 Sv/Bq | ||
| 摂取 | 成人 | 1.2x10-6 Sv/Bq | |
| 幼児 | 8.8x10-6 Sv/Bq | ||
| 排気中濃度限界(酸化物、水酸化物、硝酸塩) | 4x10-8 Bq/cc | ||
| 排気中濃度限界(それ以外) | 2x10-7 Bq/cc | ||
| 排水中濃度限界 | 6x10-4 Bq/cc | ||
ポロニウムは第1章でもお話しした、ある意味とても有名な放射性同位体です。ポロニウムが暗殺に使われる理由のひとつは、その巨大な比放射能によるものです。比放射能167TBq/gと、摂取による実効線量係数1.2×10-6Sv/Bqをかけると、1g摂取するごとの被曝量(実効線量)2.0×108Sv/gが出ます。放射線による致死量(第5章)を7Svとすると、わずか35ng(0.000000035g)でその値に達します。mgでもμgでもなく、ngです。どうですか、寿司を食べるのが恐ろしくなって来ませんか。
ふたつめは、その検知のむずかしさです。崩壊のようすを示した図を見ると、他の放射性同位体が、ラジウムのところでお話ししたように、ある確率ではγ線を出すような崩壊をし、そのγ線から放射性物質の存在を容易に検知できるのに対して、ポロニウムはほぼ100%の確率でγ線を出さない崩壊をします(γ線を出す確率は0.001%)。第4章でお話ししたように、ポロニウム210から出るα線は空気中で4cmの飛程しかありませんから、α線しか出ない放射性同位体だと、検知はとてもむずかしいのです。
喫煙によってポロニウム210を吸入してしまうことも、第1章と第6章でお話しした通りです(10)。これは、空気中を漂うラドン222が、崩壊してポロニウム218となってタバコの葉に附着し、本節の最初にお話しした過程を経て、ポロニウム210となるものです。ラドン222は気体ですのでどこからでも飛んで来ますが、タバコの肥料にリン鉱石が含まれている場合、そこにウラン238一族の同位体が比較的多く含まれている可能性が高いですから、足許がラドン222の供給源になっていることもあります。
ポロニウム210の用途として欠かせないのが、初期の核分裂兵器の起爆剤(イニシエイター)です。ポロニウム210とベリリウム9を薄い金属箔やメッキなどを隔てて設置しておき、起爆のタイミングでその箔が破れると、ポロニウム210から出たα線が、ベリリウム9と
4He + 9Be → 12C + n
という反応を起こし、中性子が発生します。この中性子が、核分裂兵器のコアの連鎖反応を引き起こすのです。ただし、これだと、ポロニウム210の半減期が138日と短いことが問題です。太平洋戦争のころのように製造してすぐに使用する場合はよいのですが、冷戦期の核兵器のように何十年も使用せずに保管するものには向いていません。そこで、現代のイニシエイターには、まったく別のメカニズムが使われています(11)。
Poloniumの語源は、こちらも第1章でお話ししたとおり、発見者のマリア・キュリーの出身地であるポーランドPolamdです。
ウラン238の娘たちはここまでにして、以降は、それ以外のα線を出す放射性同位体についてお話ししましょう。
プルトニウム239(239Pu)
プルトニウム239は、資源として利用できるほど地球上には存在していません。そこで、人工的に製造することになります。
プルトニウム239は、原子炉内でウラン238に中性子を吸収させてつくります。中性子を吸収したウラン238は、まず、ウラン239となります。ウラン239は半減期23分でβ崩壊してネプツニウム239となり、さらにネプツニウム239は半減期2.4日でβ崩壊してプルトニウム239になります。
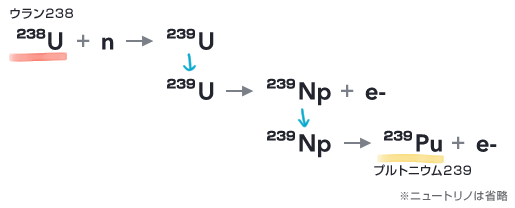
238U + n → 239U
239U → 239Np + e-
239Np → 239Pu + e-
(ニュートリノは省略)
| 実効線量係数 | 吸入 | 成人 | 1.6x10-5 Sv/Bq |
|---|---|---|---|
| 幼児 | 3.9x10-5 Sv/Bq | ||
| 摂取 | 成人 | 2.5x10-7 Sv/Bq | |
| 幼児 | 4.2x10-7 Sv/Bq | ||
| 排気中濃度限界(不溶性酸化物) | 8x10-9 Bq/cc | ||
| 排気中濃度限界(それ以外) | 3x10-9 Bq/cc | ||
| 排水中濃度限界 | 4x10-3 Bq/cc | ||
プルトニウム239は、人工的に製造する核燃料物質の代表です。ウラン235を抽出したあとの「残りかす」であるウラン238を原料として使えることも有用な上に、ウラン235よりも核分裂を起こしやすいために、核兵器の分野ではより重要になってきます。純度100%で球形の場合、核爆発を起こす臨界質量は、ウラン235が50kgていどなのに対して、プルトニウム239はわずか10kgていどです(12)。さらに反射体で覆ったりすることで、3kg以下にすることも可能です(13)。
ただ、原子炉では、生成されたプルトニウム239がさらに中性子を吸収してプルトニウム240になり、それが核兵器としての核反応を妨げますので、核兵器用のプルトニウムを製造したい場合には、プルトニウム240の割合を低く抑えるために特別な工夫が必要です(14)。
プルトニウムと言えば、日本原子力研究開発機構の大洗研究所で、保管中の容器が破裂して、作業員がその中のプルトニウムを吸入してしまった被曝事故がありました。プルトニウムが体内に入ってしまった場合には、どのように対処すればよいのでしょうか。
プルトニウムは腸からの吸収効率がとても低いので、摂取よりも吸入が問題になります。吸入し、それが「行き止まり」の肺胞にまで達した場合には、これはかなり問題になります。
不溶性の化合物の形で吸入した場合、プルトニウムは肺胞に留まり、そこから肺組織を攻撃します。これを取り除くには、肺洗浄を行います。文字通り食塩水を肺の中に入れて洗浄するのです。もちろん患者の負担は大きいです。
可溶性の化合物の形で吸入した場合、プルトニウムの一部は血液中に取り込まれて体内に入ります。体内を循環したのち、肝臓と骨に溜まりやすいことが知られています。これを取り除くことは容易ではありませんが、比較的効果的なのは、第6章でもお話ししたキレート剤を用いる方法で、ジエチレントリアミン五酢酸(DTPA)が最適なキレート剤です。
Plutoniumという名前は、ローマ神話における冥界の神Pluto(ギリシア神話のἍιδηςに相当)に由来します。原子番号の順に、ウラン、ネプツニウム、プルトニウムと並んでいますが、これは、それぞれの語源であるウラヌス、ネプチューン(海の神、ギリシア神話のΠοσειδῶνに相当)、プルートゥが、太陽系の惑星である天王星、海王星、冥王星の語源ともなっており、元素名もその惑星の順で名づけたものです。それにしても、プルトニウムが核兵器のコアの主たる材料となっていることを鑑みれば、それが「冥界の神」と名づけられているのは、とても示唆的ではありませんか。
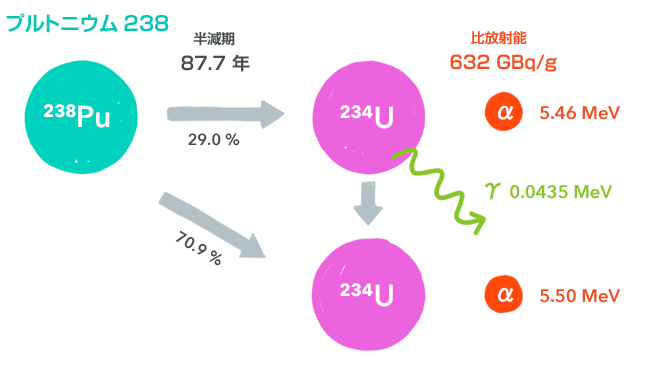
プルトニウム238(238Pu)
プルトニウム238は、プルトニウム239と質量数わずかひとつ違いの同位体ですが、似て非なるものです。そもそも、つくり方からして違います。まず原子炉内の使用済み核燃料からネプツニウム237を抽出し、それに中性子を吸収させてネプツニウム238とします。ネプツニウム238は2日の半減期でβ崩壊し、プルトニウム238になります。
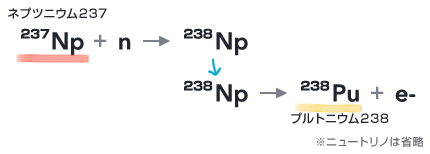
237Np + n → 238Np
238Np → 238Pu + e-
(ニュートリノは省略)
| 実効線量係数 | 吸入 | 成人 | 1.6x10-5 Sv/Bq |
|---|---|---|---|
| 幼児 | 4.0x10-5 Sv/Bq | ||
| 摂取 | 成人 | 2.3x10-7 Sv/Bq | |
| 幼児 | 4.0x10-7 Sv/Bq | ||
| 排気中濃度限界(不溶性酸化物) | 8x10-9 Bq/cc | ||
| 排気中濃度限界(それ以外) | 3x10-9 Bq/cc | ||
| 排水中濃度限界 | 4x10-3 Bq/cc | ||
用途も、プルトニウム239とはまったく違います。核燃料として用いるのではなく、放射性同位体熱電子発電機(Radioisotope Thermoelectric Generator、RTG)の熱源として用いるのです。
この原理は、ゼーベック効果という、温度差が電圧に変換される効果を利用したものです。2種類の金属(または半導体)を2箇所で接触させます。その2つの接触点に温度差があると、その間に電圧が生じる現象です。用途的には、温度を測定する熱電対がもっとも広く使われています。これの逆の効果(2つの接触点に電圧を加えると温度差ができる)を利用したものが、電子部品の冷却などにも使われているペルチェ素子です。PCを自分で組み立てる人であれば、CPUの冷却用に組み込んだりしたことがあるかも知れません。僕は半導体レーザーの温度安定化に使っていました。
これを利用して電圧を生み出すには、この接触点の片方に熱を供給し続ける熱源が必要です。その熱源として、放射性同位体の崩壊熱を利用しよう、というものです。第3章の最後のほうに、崩壊熱が意外に大きなことをお話ししましたが、それを積極的に利用したのがこの方法です。
みなさんがふだん使っている化学電池は、寿命が意外に短いでしょう。携帯電話の電池など、毎日充電しなければなりません。ところが、世の中には、そうそう簡単に電池を入れ替えたり充電したりできない環境でも、電池の需要はあるのです。たとえば、人工衛星に積む電子機器の動力源です。こういったものには、数年単位の寿命の電池が必要とされます。化学電池ではちょっとむずかしい長い期間ですが、放射性同位体を利用した電池であれば、その半減期が数十年を超えるものを選んでやれば、その間安定して電力を供給できます。第3章でお話ししたとおり、半減期は「温度や圧力といった環境では一切変化しない」のですから。
第3章の内容をもう少し思い出してください。半減期と比放射能は反比例の関係にありましたよね。ということは、「長く保つ」ことと、「大きな熱を放出する」ということは相反することで、結局は、使用目的を考えて、バランスのよいものを選ぶことになります。ポロニウム210だと熱量は大きいが寿命が短く、ウラン238だと寿命は長いが熱量は小さいのです。その絶妙なバランスということで、半減期88年のプルトニウム238が選ばれています。
第3章でのポロニウム210の場合と同様に計算すると、0.55W/gの熱を放出することになります。1kgだと550Wです。熱から電気への変換効率を考えても、電池の源としては充分な出力です。実際、これをkg単位で塊にすると、そのエネルギーで赤熱するぐらいです。二酸化プルトニウム(238)が自分自身から発する熱で赤くなっている画像をごらんください。

このプルトニウム238を利用した電池は、かつて、心臓のペイスメイカーにも内蔵されていた時代がありました。一般人が個人的に所有できる唯一のプルトニウムです。現在では、リチウム電池(充電式でないほう)に取って替わられています。ペイスメイカーはそれほどの電力を消費しないからです。人工衛星用の電池としては、今もプルトニウム238を使った電池が活躍しています。
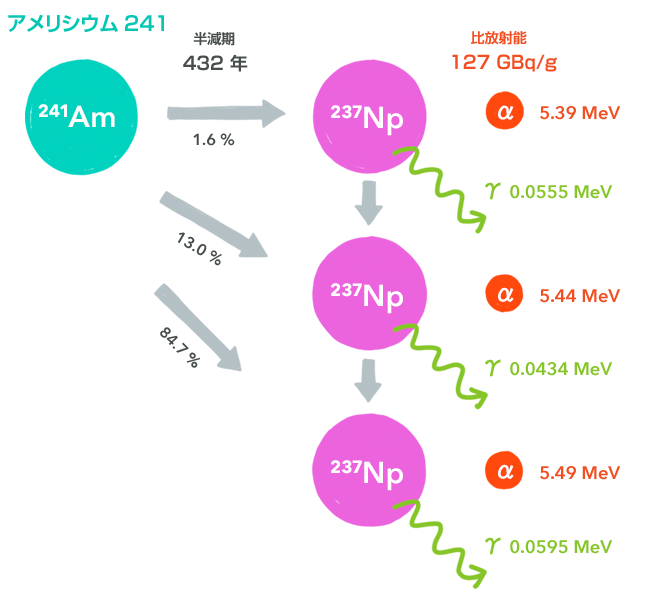
アメリシウム241(241Am)
原子炉の中でウラン238が中性子を吸収して段階を踏んでプルトニウム239になるという話をしましたが、それをそのまま原子炉に入れたままにして運転を続けると、やがてその一部はさらに中性子を吸収してプルトニウム240となります。それがさらに中性子を吸収すると、プルトニウム241になります。このプルトニウム241は半減期14.3年でβ崩壊を起こしてアメリシウム241になります。

239Pu + n → 240Pu
240Pu + n → 241Pu
241Pu → 241Am + e-
(ニュートリノは省略)
| 実効線量係数 | 吸入 | 成人 | 1.6x10-5 Sv/Bq |
|---|---|---|---|
| 幼児 | 4.0x10-5 Sv/Bq | ||
| 摂取 | 成人 | 2.0x10-7 Sv/Bq | |
| 幼児 | 3.7x10-7 Sv/Bq | ||
| 排気中濃度限界 | 3x10-9 Bq/cc | ||
| 排水中濃度限界 | 5x10-3 Bq/cc | ||
Americiumの名前は、その響きからすぐにわかるように、アメリカから取られています。アメリカでの最大手のスーパーマーケットはウォルマートですが、このアメリシウムは、「ウォルマートでも買える放射性物質」とでも呼ぶべきものです。ただし「アメリシウム241」と札が貼られて売られているわけではありません。ウォルマートで売っているのは煙感知器で、その中にアメリシウム241が使われているのです。
この感知器は、イオン化式煙感知器と呼ばれています。イオン化式、つまり電離式です。放射線が空気分子を電離することは第4章でお話ししましたし、その電離されたイオンを測定することで放射線量を測定するものとして第7章で電離箱をご紹介しました。その電離箱を応用したものが、このイオン化式煙感知器です。![]()
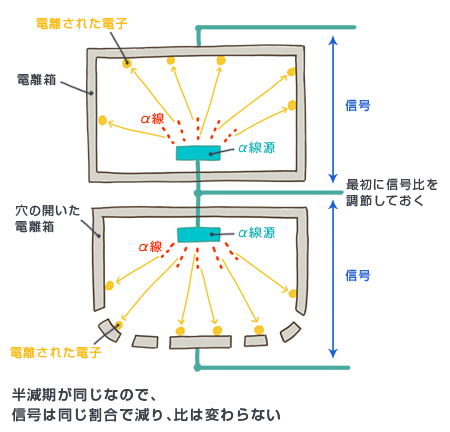
最初に電離箱と穴の開いた電離箱との信号比を調節しておく
半減期が同じなので、信号は同じ割合で減り、比は変わらない
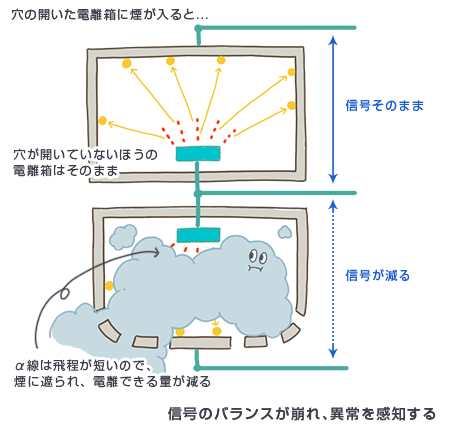
穴の開いた電離箱に煙が入ると、α線は飛程が短いので、煙に遮られ電離できる量が減る。穴が開いていないほうの電離箱はそのままなので信号のバランスが崩れ、異常を感知する
感知器のコアは、放射性物質を中に入れた電離箱です。放射性物質が内蔵されているわけですから、この電離箱は常に放射線を検出し続けていることになります。その電離箱には、穴が開いています。この穴から中に煙が入ると、α線は煙に遮られ、電離する空気分子の量が減ってしまいます。電離箱は放射線量を電流に変えて検出するわけですから、電流が減れば警報を鳴らすようにしておけばよいわけです。
ところが、そのままだとうまく使えません。放射性物質は放射線を出すことで減っていくわけですから、煙がなくとも、放射線量、つまり電離量は自然に減っていくからです。そこで、密閉されているということ以外は同じ構造の電離箱を電気的につなぎ、その信号の比を見るのです。そうすれば、密閉されたほうも煙が入ってくるほうも同じ割合で放射線量は減っていきますから、煙が入ることで自然減少分よりも余計に減った分だけを検出できます。
この放射性物質に、アメリシウム241が使われています。現在、日本では放射性物質を使わない方式の煙感知器が使われていますが、欧米ではまだまだこのイオン化式煙感知器が多く使われています。
1974年、ハンフォード(アメリカの核施設)にて、アメリシウム241による被曝事故が起こりました(15)。この事故では、アメリシウム241を吸着したイオン交換樹脂の容器が破裂し、その破片が作業者の顔面に刺さったために、その傷口から大量にアメリシウム241が体内に取り込まれたという、極めて特殊な事故です。このときの対処としては、傷口の洗浄のほか、体内に取り込まれてしまった分に対しては、プルトニウムのところにも登場したキレート剤、ジエチレントリアミン五酢酸(DTPA)が投与されました。なんと1年半もの間、投与を続けたそうです。その効果があり、当時の許容量の1万倍もの量を取り込んだにもかかわらず、急性障害を防ぐことができたのでした。
カリフォルニウム252(252Cf)
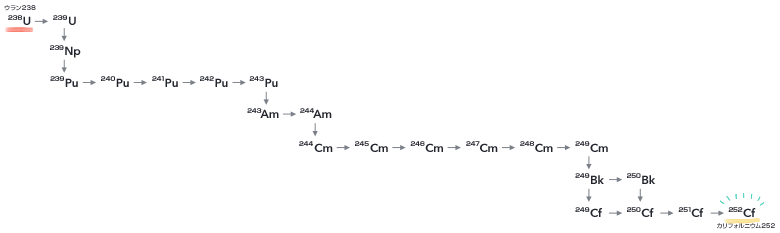
カリフォルニウムも天然資源として存在せず、人工的につくることになるのですが、これをつくるのは相当たいへんです。天然資源でもっとも質量数が大きなものは、これまでお話ししたとおりウラン238で、だからこそすべての母たりえるのですが、それより質量数が大きなものは、これに中性子をくっつけていってつくり出すことになります。第1章でも本章でもお話しした、現代の錬金術ですね。プルトニウム239やアメリシウム241のような、ウラン238とほとんどおなじ質量数のものはそれほどむずかしくないのですが、252という質量数は、238よりはるか先にあります。中性子をひとつずつ時間をかけてくっつけていくので、とても遠い道程です。しかも、途中の生成物は、とても寿命が短いものも多く、どんどん壊れていきますから、その壊れる分も見込んでたくさんつくらねばなりません。ですから、カリフォルニウム252は、1gあたり何十億円もするほど高価です。僕はもちろん買ったことはありませんが。
ウラン238からスタートしてカリフォルニウム252へと至る経路をいちおう書いておきます。
どうですか、気が遠くなる道程でしょう。このような手間をかけてなお求められるのは、カリフォルニウム252がある重要な性質をもっているからです。
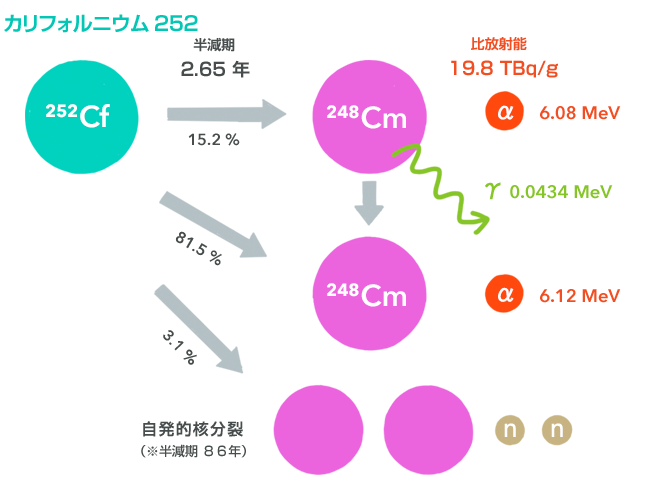
半減期: 2.65年 比放射能: 19.8TBq/g
自発的核分裂の半減期: 86年
※ 核分裂によってどのような原子核が生じるかは、とてもたくさんのパターンがありますので、この図では生成した原子核の記号を特に書いてありません
※一番下の反応は核分裂であり、核分裂は下の「β線を出す放射性同位体」のところでも書いてありますように、核分裂によってどのような原子核が生じるかは、とてもたくさんのパターンがありますので、この図では、生成した原子核の記号を特に書いてありません
| 実効線量係数 | 吸入 | 成人 | 2.0x10-5 Sv/Bq |
|---|---|---|---|
| 幼児 | 8.7x10-5 Sv/Bq | ||
| 摂取 | 成人 | 9.0x10-8 Sv/Bq | |
| 幼児 | 5.1x10-7 Sv/Bq | ||
| 排気中濃度限界 | 6x10-9 Bq/cc | ||
| 排水中濃度限界 | 7x10-3 Bq/cc | ||
この崩壊の図が、他の放射性同位体のものと大きく異なることがおわかりになるでしょうか。それは、「自発的核分裂」というものが入っているからです。自発的核分裂は、外から中性子を吸収しなくても、その原子核が勝手に分裂してしまう現象のことです。実はウラン以上の巨大な質量数をもつ同位体は、ある確率で自発的核分裂を起こします。しかし本章の図では、基本的に1%以上の確率で起こるものだけを描きましたので、他の同位体のところには描かれていません。カリフォルニウム252だけに自発的核分裂が描かれているのは、それだけ高い頻度で起こることを意味しています。これまで話題に上がった同位体の、1gあたり、1秒あたりの自発的核分裂の頻度を並べてみます(16)。
| 235U | 0.0000056 Bq/g |
|---|---|
| 238U | 0.0068 Bq/g |
| 238Pu | 1,170 Bq/g |
| 239Pu | 0.007 Bq/g |
| 240Pu | 482 Bq/g |
| 241Am | 0.46 Bq/g |
| 252Cf | 610,000,000,000 Bq/g |
どうですか、カリフォルニウム252が突出していることがわかるでしょう。
核兵器や原子炉に用いる核燃料は、人間が望むタイミングで核分裂を起こしてくれないと困ります。ですから、外部から中性子を与えられたときに核分裂を起こし、そうでない場合に、つまり自発的に核分裂を起こすことは、できるだけないほうがよいのです。その点では、ウラン235がいかに優秀な核燃料であるかがわかります。そして、プルトニウム239のところで、プルトニウム240が混ざる量が多くなると望ましくないということをお話ししたのも、プルトニウム240の自発的核分裂の頻度が高いからです。
しかし、そんなプルトニウム240など問題にならないほどの頻度で自発的に核分裂を起こすのが、カリフォルニウム252なのです。
ですから、カリフォルニウム252は、核燃料としてはまったく使えないことになります。
ところが、捨てる神あれば拾う神あり、です。そんなカリフォルニウム252でも、逆にその自発的核分裂の頻度が圧倒的に高いことを利用して、あることに利用されています。それが中性子源としての利用です。
もう一度崩壊のようすを表わした図をごらんいただくと、原子核が分裂していると同時に、中性子も発生していることがわかります。核分裂の破片として、原子核だけでなく、中性子も出て来るのです。第8章のJCO臨界事故の話のところで、駆け足ではありましたがかんたんに連鎖反応についてお話ししましたが、そこでも、核分裂の際に中性子が飛び出すことをご説明しました。つまり、カリフォルニウム252は、核分裂のエネルギーを利用するのではなく、核分裂によって生じる中性子を利用するのです。
カリフォルニウム252の中性子源としての利用は、ひとつには非破壊検査への利用があります。X線撮影と同様にして、透過しやすいしにくいの違いを利用して、中身を調べるものです。中性子と物質との反応はX線のそれとはとはまったく違った様相を呈しますので、それを積極的に利用して、X線ではわかりにくいものを調べることができます。
そしてなんと言っても、原子炉の反応を開始させるイニシエイターとしての役割が重要です。イニシエイターについてはポロニウムのところでも触れましたが、連鎖反応を起こすための最初の中性子を発生させる中性子源のことです。
Californiumの語源は、それを発見した物理学者たちが所属していたカリフォルニア大学バークリー校です。この大学は物理学の分野ではアメリカ三大名門大学とも言うべきところ(残りふたつは、プリンストン大学とマサチューセッツ工科大学)で、バークリーから取られた元素名バークリウムまであるほどです。マンハッタン計画のリーダーにしてロスアラモス国立研究所初代所長であるユリウス・ロベルト・オッペンハイマーや、このカリフォルニウムをはじめ10個もの元素を発見したグレン・セオドア・シーボーグもここで教鞭をとっていました。本章で紹介した元素では、プルトニウムとアメリシウムとカリフォルニウムがシーボーグによる発見です。
β線を出す放射性同位体
α線の次はβ線を放出する放射性同位体を見ていきましょう。
まずは原子炉の燃え残りからです。ウラン235やプルトニウム239は、原子核が分裂する「核分裂」という現象を起こすことで、エネルギーを生み出しています。つまり、原子炉が運転されると、ウラン235やプルトニウム239が分裂してできた「破片」の原子核がつくられていくのです。
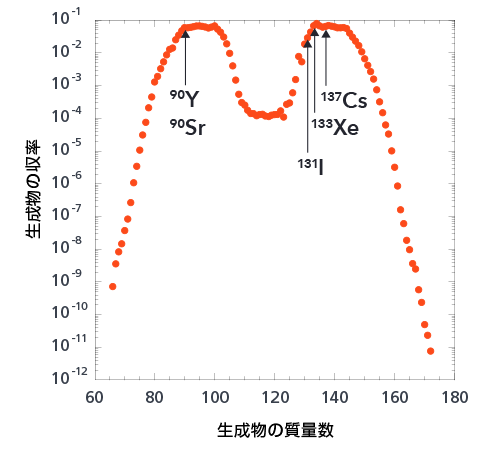
図は、ウラン235が0.025eVのエネルギーの中性子(一般的な原子炉内での中性子)を吸収して核分裂したときの「破片」、つまりウラン235から新たに生まれた原子核の生成率を表わしたものです(17)。ちょうど半分(質量数118)のところは谷間になっていて、真っ二つに割れるというよりも、大きめの破片と小さめの破片とに分裂するようすがわかるかと思います。生成物の収率、ということからもわかりますように、どの原子核に分かれるかはまさに確率的で、実際の原子炉の中では、このすべての種類の原子核が新たに生まれていることになります。
ここで、第1章の最後のほうの、安定な原子核での陽子と中性子の数の比率についての話を思い出してください。「小さな原子核では、陽子と中性子はほぼ同じ数だが、強い力は隣り合う核子同士にしか働かないために、大きな原子核ほど、中性子を多めに必要とする」という話でした。つまり、ウラン235やプルトニウム239といった巨大な原子核では、中性子がかなり多めに入っているのですが、それが半分くらいの大きさの原子核に分かれると、中性子はそれほど必要でないので、「中性子が多すぎる原子核」となってしまうのです。その原子核がどうなるのかは、第2章でお話ししたとおりです。β崩壊によって中性子を陽子に変え、陽子と中性子のバランスをよくしようとします。ですから、結局のところ、核分裂によってつくられたものは、β線を出す放射性同位体になる、ということです。これが、原子炉がその運転によって放射性物質を生みだす仕組みです。
我々は、自分たちの快適な生活や豊かな暮らしの代償に放射性物質を生みだしている、ということも、決して忘れてはなりません。
では、ここからは、まず核分裂によって生みだされた放射性同位体から始めましょう。
セシウム137(137Cs)
福島第一原子力発電所事故によって一躍有名となった放射性同位体のひとつが、このセシウム137です。セシウムは、セシウム133のみが安定した同位体で、それ以外の同位体はもともと地球上にはほとんどありませんので、人類が核分裂を起こさなければ、そしてそれが外に漏れなければ、みなさんが出逢うこともなかったものです。でも、福島第一原子力発電所事故以前には環境中にまったくなかったのかというと、そうではありません。国連の安全保障理事会の常任理事国が、盛んに大気内核実験を行っていた時期があるからです。その時期に地上にばらまかれたセシウム137が、今もたくさん残っています。
| 実効線量係数 | 吸入 | 成人 | 3.9x10-8 Sv/Bq |
|---|---|---|---|
| 幼児 | 1.0x10-7 Sv/Bq | ||
| 摂取 | 成人 | 1.3x10-8 Sv/Bq | |
| 幼児 | 1.2x10-8 Sv/Bq | ||
| 排気中濃度限界 | 3x10-5 Bq/cc | ||
| 排水中濃度限界 | 9x10-2 Bq/cc | ||
セシウムは、化学的には、アルカリ金属に属するため、それらと非常によく似た性質を持っています。アルカリ金属と言えば、ナトリウムやカリウムがそうですが、どちらも我々の身体に欠かせない元素です。それらと同じ仲間であるために、体内での挙動も似ています。アルカリ金属はとても水に溶けやすいので、腸からの吸収率もとても高いのが特徴で、一方で、まさにその溶けやすさから、体外にも排出されやすくなっています。ですから、第5章でお話しした通り、30年という物理学的半減期よりも、生物学的半減期のほうがはるかに短いです(18)。
水に溶けやすいことから、環境中に存在する場合でも、水とともに移動しやすいです。第7章で、福島第一原子力発電所事故直後には、我々の研究施設内の道路の表面でもたくさん検出されたことをお話ししましたが、それも、間もなく検出されなくなりました。とくに除染もなにもしていないにもかかわらず、です。つまり、雨に流されてしまったということを意味しています。勿論これも第6章でお話ししたとおり、なくなってしまったわけではなく、排水溝から川へ、そして海へと流されてしまっただけです。
このことから、吸入よりも経口摂取に気をつけるべき放射性同位体です。食事の前によくよく手を洗いましょう。たったそれだけのことを怠ったために生死を分けた例を、第8章でお話ししました。
セシウム137が体内に入ってしまった場合の除去方法は、第6章でお話ししたイオン交換体を投与するものが有効です。セシウムの場合はヘキサシアノ鉄(II)酸鉄(通称プルシアンブルー)を投与し、それがセシウムを捕らえることを利用し、それごと体外に排出させます。第8章のゴイアニア事故でも、内部被曝が疑われる人には、プルシアンブルーが投与されました。
caesium(ラテン語、英語ではcesium)の語源は、ラテン語のcaesiusで、青みがかった灰色のことだそうです。これは、発光スペクトル(軌道上電子からの光であって、γ線ではありませんよ、念のため)の輝線が青いことがその由来だそうです。
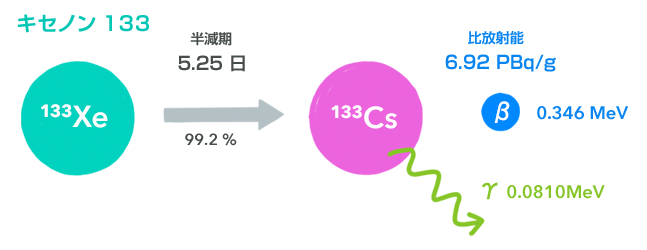
キセノン133(133Xe)
キセノン133も核分裂生成物ですが、他の生成物と違うのは、これが気体であるということです。
| 排気中濃度限界 | 2x10-2 Bq/cc | ||
|---|---|---|---|
地上核実験を行っていたおおらかな時代と違い、現在はそれが禁じられ、核実験は地下の実験施設で行われます。そのため、核分裂生成物は実験施設に閉じ込められますが、気体を閉じ込めるのはとても難しいので、これだけは地上に漏れ出します。そして、一旦地上に漏れ出した気体は、気流に乗って広範囲に拡散されますから、その実験場から離れた場所でも観測されることがあります。北朝鮮が核兵器実験を行ったかどうかを判断するのも、このキセノン133が検出されたかどうかで判断することもあります。実験場の近くには行けなくとも、気流に乗って拡散した気体を収集することは可能だからです。
キセノン133は、トレイサーとしても利用されています。キセノン133は貴重な気体のトレイサーですので、肺での換気機能を調べるのに使われています。81keVという低いエネルギーのγ線がここでは役に立っています。
ところでみなさんの中には、キセノンと言われて最初に思い浮かべるのがキセノンランプである人もおられるのではないでしょうか。あの夜目にも眩しい自動車のヘッドライトがそれです。キセノンランプはキセノン雰囲気中での放電を利用したものですが、点灯時のみその放電を利用したものも広義的には含まれます。同様に気体中の放電を用いたランプには、ヘリウム、ネオン、アルゴン、クリプトンを用いたものがありますが、キセノンを含めて、これらはすべて、希ガスと呼ばれる元素の仲間に属します。周期表で言うと一番右端の列です。ラドンも希ガスです。ランプには使いませんが。
希ガスは、化学的な反応性に乏しい、つまり化学的に安定した気体ですので、ランプ以外にも、その安定性を利用した用途に広く使われています。
キセノン133以外のキセノンの放射性同位体としては、キセノン135が有名で、これは原子炉の運転によって生成する同位体であるにもかかわらず、中性子の吸収断面積が極めて高いのが特徴です。一般的な原子炉内での代表的な速度(0.025eV)の中性子に対する吸収断面積(19)は、水素1で0.33b、炭素12で0.0035b、吸収剤として有名なホウ素10で3,800bであるのに対して、キセノン135はなんと2,900,000bもあります(20)。このため、原子炉の運転を妨げる物質(「毒物質」と呼ばれます)として、特に扱いに注意を要します。運転とともに炉内に発生するので、あらかじめ取り除いておく、ということができないからです。史上最悪の原子力事故であるチェルノブイリ原子力発電所事故の原因も、運転員がこのキセノン135に起因する原子炉の挙動に対する対応を誤ったためです。
Xenonの語源は、ギリシア語のξένον(奇妙な)です。日本人は「キセノン」と発音しますが、英語ではゼノンです。![]()
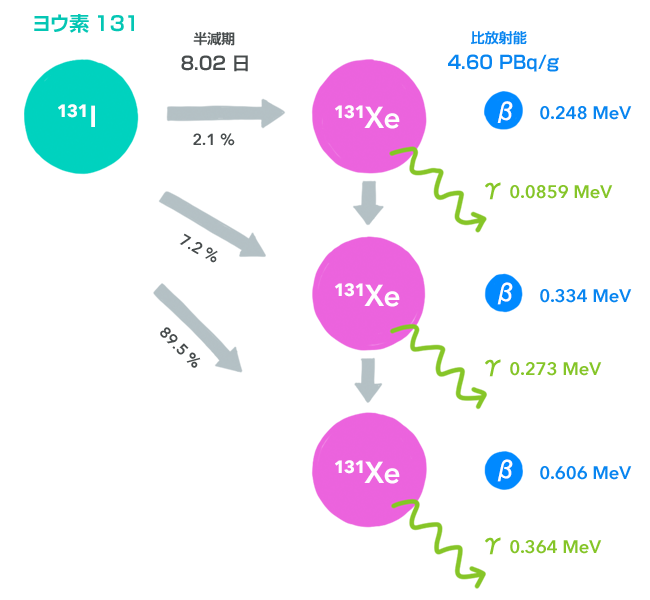
ヨウ素131(131I)
ヨウ素131は、福島第一原子力発電所事故以前に、チェルノブイリ原子力発電所事故で一躍有名になった放射性同位体です。
| 実効線量係数 | 吸入 | 成人 | 1.6x10-9 Sv/Bq |
|---|---|---|---|
| 幼児 | 6.2x10-9 Sv/Bq | ||
| 摂取 | 成人 | 2.2x10-8 Sv/Bq | |
| 幼児 | 1.8x10-7 Sv/Bq | ||
| 排気中濃度限界(蒸気) | 5x10-6 Bq/cc | ||
| 排気中濃度限界(ヨウ化メチル) | 7x10-6 Bq/cc | ||
| 排気中濃度限界(それ以外) | 1x10-5 Bq/cc | ||
| 排水中濃度限界 | 4x10-2 Bq/cc | ||
ヨウ素は海藻に多く含まれているため、海藻をよく喰べる日本人はその摂取量が他国に比べて多いです。内陸国ではヨウ素欠乏症になる人が比較的多く、逆に日本ではヨウ素の過剰摂取によるものと思われる海岸性甲状腺腫を発症する人もいます。
ヨウ素の工業的な生産では、全世界のうち、1位のチリが2/3、2位の日本が1/3と、驚くべきことにこの2カ国でほとんどを占めます。資源が乏しいと言われ続けている日本で、このような輸出資源があるということは意外なことでしょう。しかも、日本での生産のうち、そのほとんどが、千葉県で産出しているのです。![]() これは南関東ガス田という天然ガス鉱床から抽出しているのですが、そもそもこんなところにガス田があったということをごぞんじなかった方も多いのではないでしょうか。このガス田は、可採埋蔵量4,000億m3にも及び、日本の天然ガス埋蔵量の実に9割を占めると言われています(21)。
これは南関東ガス田という天然ガス鉱床から抽出しているのですが、そもそもこんなところにガス田があったということをごぞんじなかった方も多いのではないでしょうか。このガス田は、可採埋蔵量4,000億m3にも及び、日本の天然ガス埋蔵量の実に9割を占めると言われています(21)。
ヨウ素は半減期が8日ととても短いため、事故などで生活環境中に漏れた場合には、最初の数日の対応がとても大切になってきます。チェルノブイリ原子力発電所事故では、このヨウ素に対する初期対応(ヨウ素剤云々以前に、飲み物に気をつけるなど)が遅れたために、周辺住民の甲状腺癌の発生が有意に増えました(22)。そう、ヨウ素は甲状腺に溜りやすいのです。それを逆に利用して、バセドウ病の治療のためにヨウ素131を投与して故意に被曝させる話も、第9章でしました。
ヨウ素131が体内に入った場合、もしくは入る恐れがある場合の対処方法は、第6章でもお話ししたとおり、放射性でないヨウ素の同位体を投与することで、体内の全ヨウ素中のヨウ素131の割合を下げる方法です。みなさんも、福島第一原子力発電所事故が起こった直後に「ヨウ素剤を飲め」なる話を聞いたことがあるではないでしょうか。さきほどお話ししたとおり、日本人は普段からヨウ素の摂取量が多いのでそれほどでもありませんが、大陸国の人たちは普段の摂取量が少ないだけに、ヨウ素剤の摂取はとても効果的です。
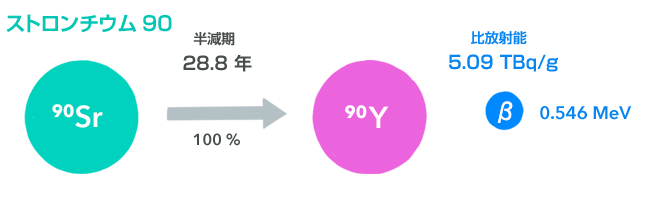
ストロンチウム90(90Sr)
福島第一原子力発電所事故の際に、セシウム137やヨウ素131と並んで有名になったのが、このストロンチウム90です。
| 実効線量係数 | 吸入 | 成人 | 1.6x10-7 Sv/Bq |
|---|---|---|---|
| 幼児 | 4.0x10-7 Sv/Bq | ||
| 摂取 | 成人 | 2.8x10-8 Sv/Bq | |
| 幼児 | 7.3x10-8 Sv/Bq | ||
| 排気中濃度限界(チタン酸ストロンチウム) | 8x10-7 Bq/cc | ||
| 排気中濃度限界(それ以外) | 5x10-6 Bq/cc | ||
| 排水中濃度限界 | 3x10-2 Bq/cc | ||
ストロンチウム90は崩壊の仕方がひと通りで、しかもβ線だけを出すので、とてもわかりやすいです。ストロンチウム90が崩壊してできたイットリウム90は、まだ不安定な放射性同位体の状態ですので、それについては次節で取り上げておきます。
ストロンチウムはカルシウムと同じアルカリ土類金属ですので、体内では、カルシウムが集まるところに同じように集まります。つまり骨です。
体内に取り込まれてしまったストロンチウム90を取り除くのは、とてもむずかしいです。体内の特定箇所に溜まりやすいものといえばヨウ素が思い浮かぶかも知れませんが、ストロンチウム90を取り除く方法として、ヨウ素と同じような方法は採れません。なぜなら、ストロンチウムはカルシウムと間違えて骨に取り込まれるので、相対的な濃度を下げるにしても、体内のカルシウム量は相当に多いので、それに対する濃度を薄めようとすると、大変な量の非放射性ストロンチウムを投与しなければならず、現実的ではありません。
そこで、第6章でもお話ししたように、代謝を攪乱させる方法を採ります(23)。カルシウムの量が少ない食事を続けると、骨からカルシウムが離脱し、ストロンチウム90も離脱していきます。いっぽう、離脱したストロンチウム90を腎臓から排出させるには、リンの量が少ない食事を続けるのがよいです。ただし、それだけだと、カルシウム量の低下を察知した身体が腎臓からの排出を抑制するように動くので、代わりに、放射性同位体でないストロンチウムを摂取させます。この、低カルシウム・低リン・高ストロンチウム(非放射化)食の組み合わせが、骨に入ってしまったストロンチウム90を除去するのに最適なものとなります。ただし、カルシウムを不足させて代わりにストロンチウムを摂取させていることになるので、長期間の適用は障害を引き起こします。したがって、あくまでストロンチウム90をある程度排出させるための短期間の処置です。
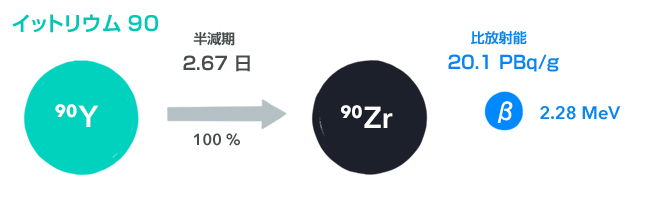
イットリウム90(90Y)
イットリウム90は、それ単独ではそれほど有名でもないのですが、ストロンチウム90の娘であり、半減期もわずか2.7日と短いので、ストロンチウム90の影響とまとめて扱われることが多いです。
| 実効線量係数 | 吸入 | 成人 | 1.5x10-9 Sv/Bq |
|---|---|---|---|
| 幼児 | 8.8x10-9 Sv/Bq | ||
| 摂取 | 成人 | 2.7x10-9 Sv/Bq | |
| 幼児 | 2.0x10-8 Sv/Bq | ||
| 排気中濃度限界 | 8x10-5 Bq/cc | ||
| 排水中濃度限界 | 3x10-1 Bq/cc | ||
つまり、ストロンチウム90を体内に取り込んでしまうと、ストロンチウム90からのβ線だけでなく、イットリウム90からのβ線も浴びることになります。しかもイットリウム90からのβ線のほうがはるかにエネルギーが高いです。
イットリウムになってしまうと、化学的な挙動はストロンチウムとまったく異なりますので、体内からの除去の方法もまったく異なります。イットリウムの除去には、第6章でお話ししたキレート剤を使います。プルトニウムやアメリシウムのところでもお話ししたジエチレントリアミン五酢酸(DTPA)は、イットリウムに対しても有効です。
イットリウムはみなさんに取っては縁遠い物質かも知れませんが、僕は学部生のときの実験で扱ったことがあります。イットリウム、バリウム、銅、酸素の化合物であるYBa2Cu3O7は、比較的高い温度(90K以上)で超伝導となる物質で、この温度は液体窒素で冷却して達成できるので、超伝導の実験ではよく使われるのです(もっとも広くつかわれている超伝導物質であるニオブチタンで10K)。僕も、大学3年生のときに、自分で酸化イットリウムと炭酸バリウムと酸化銅を混ぜて焼き固めてこれをつくりました。
他には、産業に詳しい方であれば、YAGレーザーというものをごぞんじかも知れません。これは、イットリウム・アルミニウム・ガーネット(Yttrium Aluminum Garnet)の結晶(化学式はY3Al5O12)を媒質に用いたレーザーで、工業用レーザーとして広く使われています。
Yttriumの語源は、それを含む鉱物が発見された場所であるスウェーデンのイッテルビー(Ytterby)に由来します。
使用済み核燃料に含まれる放射性同位体はここまでにして、ここからはそれ以外で重要なβ線を出す放射性同位体についてみていきましょう。
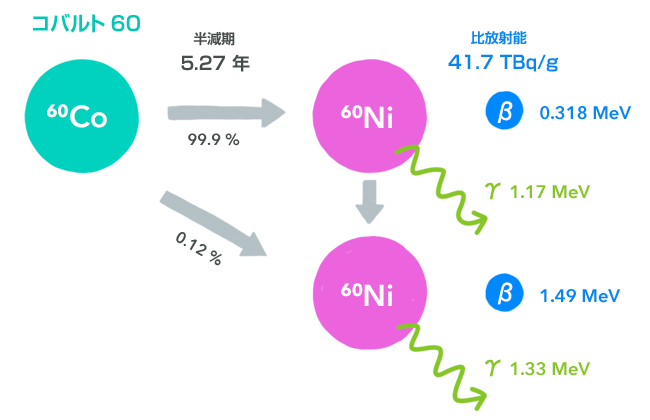
コバルト60(60Co)
コバルト60は、工業的医療的利用のために人工的につくられる放射性同位体の代表格です。
天然のコバルトは、100%コバルト59です。これに原子炉で中性子を照射し、吸収させて、コバルト60を製造します。
| 実効線量係数 | 吸入 | 成人 | 3.1x10-8 Sv/Bq |
|---|---|---|---|
| 幼児 | 8.6x10-8 Sv/Bq | ||
| 摂取 | 成人 | 3.4x10-9 Sv/Bq | |
| 幼児 | 2.7x10-8 Sv/Bq | ||
| 排気中濃度限界(酸化物、水酸化物、ハロゲン化物、硝酸塩) | 4x10-6 Bq/cc | ||
| 排気中濃度限界(それ以外) | 1x10-5 Bq/cc | ||
| 排水中濃度限界 | 2x10-1 Bq/cc | ||
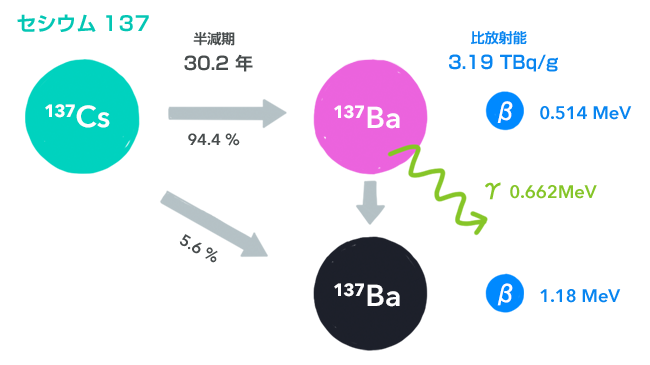
図のようにコバルト60は99.9%が2段階の崩壊をしますから、観測する側としては、1.17MeVと1.33MeVの2本のγ線を放出したように見えます。このγ線が、γ線照射源としてはもっとも広く利用されるものです。第9章でお話しした食品へのγ線照射やγ線滅菌、そしてγ線照射による治療にも、このコバルト60が使われます(24)。
我々は、実験施設の建設の際に各種材質の耐放射線性能を調べましたが、そのために原研の高崎研究所(当時、現在は原研から切り離され、量子科学技術研究開発機構に編入されています)の照射施設に行って照射試験を行いました。そこでもγ線源としてコバルト60が使われていました。
このように広く利用されているだけに、事故もそれなりに起こっています。多くは、工業や医療目的で使用されたコバルト60が、それを含む装置ごとスクラップにされ、スクラップに混ざった状態で再利用されてしまうことです。一例として、メキシコで起きた事故について触れておきましょう(25)。
1977年、メキシコのヤレスの医療センターが、アメリカから中古のコバルト60入り放射線治療機器を購入しました。しかし、ヤレスの医療センターでは使用されずに倉庫に保管されていました。1983年11月に、窃盗犯がその倉庫から盗み出し、12月にスクラップ業者に売り飛ばしました。ゴイアニア被曝事故と似ていますが、ここでも、窃盗犯には放射線に関する知識はなかったようです。
スクラップ業者はコバルト60を含む屑鉄を鉄製品業者に販売し、鉄製品業者はその屑鉄から鉄製品をつくってメキシコ国内とアメリカに販売しました。
1984年1月、その鉄製品を運んでいたトラックが、たまたま、ロスアラモス国立研究所(アメリカの核兵器開発のためにつくられた研究所)の前を通過しようとし、敷地境界の放射線測定器を反応させ、事件が発覚しました。製品の納入先はロスアラモス研究所ではなく、まったく違うところであり、同研究所の前を通ったのは本当にたまたまですから、この偶然がなければ発覚はもっともっと遅れていたでしょう。
コバルトは、無機化合物の状態では体内に吸収されにくいのですが、有機化合物の場合には取り込まれやすくなります。特にビタミンB12の構成要素ですので、人体に取っての必須元素でもあります。ビタミンB12が欠乏すると、DNA合成障害が起き、悪性貧血となります。
産業的には、他の金属とともに鉄に混ぜられ、耐摩耗性が高い合金をつくります。みなさんがホームセンターに行くことがあれば、是非、工具コーナーに行ってみてください。ドリルの刃の材質は、多くがコバルト合金です。また、アルミニウムやニッケルとの合金は、アルニコ磁石と呼ばれる強力な磁石となります。
ウランのところでアトムの妹のウランちゃんの話をしましたが、アニメ版には、コバルト兄さんというのも登場しました。原作ではアトムの弟だそうですが。ウランとともに、放射性同位体の代表格として当時はとらえられていたことがわかります。コバルトの語源は、ドイツ語圏の妖精のコボルト(kobold)です。
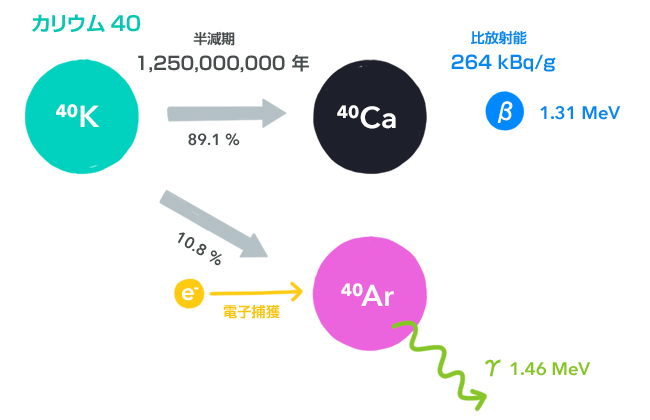
カリウム40(40K)
カリウム40は、本章でご紹介した放射性同位体の中でウラン238に次いで寿命が長く、太古の昔からずっと存在してきているものです。
| 実効線量係数 | 吸入 | 成人 | 2.1x10-9 Sv/Bq |
|---|---|---|---|
| 幼児 | 1.7x10-8 Sv/Bq | ||
| 摂取 | 成人 | 6.2x10-9 Sv/Bq | |
| 幼児 | 4.2x10-8 Sv/Bq | ||
| 排気中濃度限界 | 5x10-5 Bq/cc | ||
| 排水中濃度限界 | 1x10-1 Bq/cc | ||
カリウム40の崩壊の仕方は特徴的です。他の同位体が何通りかの崩壊の仕方をしても、それは途中で「寄り道」するだけで、結局は同じところに行き着くのであるのに対して、カリウム40は、カルシウム40とアルゴン40という、まったく違う2種類の同位体に変化します。そして、それぞれの崩壊も、β-崩壊と電子捕獲と、まったく違います。
第6章でもお話ししたように、カリウムは人体に取って必須の、それもかなりの量が必要な元素ですので、体内に含まれるのはもう避けられません。内部被曝が嫌で摂取をしないとなると、普通に死んでしまいます。
カリウムの役割は重要ですが、特に神経伝達には欠かせないものです。細胞の内外では、カリウムイオンの濃度が大きく異なるように維持されており(内部が高く、外部が低い)、それによって細胞内外で電位差(電圧)が生じます。その電位差の変化を伝えることで、情報を伝達しているのです。
そのため、体内のカリウム濃度が急激に変化すると、最悪の場合には心停止に至ります。死刑の一種である薬殺刑では、塩化カリウムを注射しますし、一時期社会問題にもなったタナトロンという自殺装置も、塩化カリウムを点滴するものです。このように、身体にとってなくてはならないものでも、量が適切でないと死に至ることもあるのです。何事においても、大切なのは量の問題であるという、典型的な例です。
カリウムというのはドイツ語(Kalium)で、英語ではPotassiumです。元々は植物の灰を意味するアラビア語(القَلْيَه)が語源で、植物の灰からカリウムを抽出していたのが由来です。ちなみに、このالقَلْيَهは、「アルカリ」の語源でもあります。カリウムがアルカリの代表格であることがわかります。
炭素14(14C)
炭素14は、大気中の窒素14(ごく普通の窒素)が中性子を吸収し、
14N + n → 14C + p
という、中性子と陽子が入れ替わる反応によってつくられます。中性子は宇宙線と大気との反応によってつくられますので、この反応は絶えず起こっていて、炭素14は安定した供給を受けていることになります。
| 実効線量係数 | 吸入 | 成人 | 5.8x10-9 Sv/Bq |
|---|---|---|---|
| 幼児 | 1.7x10-8 Sv/Bq | ||
| 摂取 | 成人 | 5.8x10-10 Sv/Bq | |
| 幼児 | 1.6x10-9 Sv/Bq | ||
| 排気中濃度限界(蒸気) | 2x10-4 Bq/cc | ||
| 排気中濃度限界(一酸化物) | 1x10-1 Bq/cc | ||
| 排気中濃度限界(二酸化物) | 2x10-2 Bq/cc | ||
| 排気中濃度限界(メタン) | 5x10-2 Bq/cc | ||
| 排水中濃度限界 | 2 Bq/cc | ||
大気中でつくられた炭素14は、二酸化炭素の形で植物に取り込まれ、食物連鎖によって動物の身体にも常時取り込まれています。炭素は、生物の身体を構成するもっとも基本的な元素ですから、摂取を控えるとか、体内から取り除くとか、そういうこと以前のものです。ありとあらゆる生物の中に、この放射性同位体は含まれています。
そのことを利用したものが、第9章でお話しした、炭素14を使った年代測定です。あらゆる生物が必ずある一定量を含んでいるからこそ可能な方法です。
しかし、何度かお話ししているように、40~60年代には、国連の中核を成す安全保障理事会常任理事国が、遠慮なしに地上で核実験を行っていましたから、そのときに大量に放出された中性子によって、炭素14も自然生成分よりも多めにつくられました。そのため、年代測定を行うときには、この核実験の分の補正を行う必要があります。ほんと、国連は碌なことをしないですね。
Carbonの語源は、木炭を表わすラテン語carboに由来します。
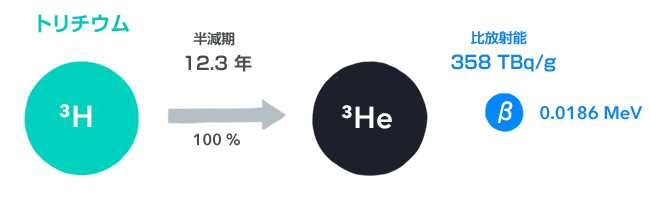
トリチウム(3H)
トリチウムは水素の同位体で特別に名前をつけてもらっているものですが、Tritiumという名前が表わすように、核子が3つあるものです(triはラテン語で3を意味します)。そのため、日本語では「三重水素」という名前もつけられています。その3つの核子は、陽子1つと中性子2つです。中性子が多すぎるためにβ崩壊を起こします。
トリチウムは、デューテリウム(水素2)が中性子を捕獲することでできます。
2H + n → 3H
そのため、中性子が発生するところでは、かならずと言っていいほど生成される同位体です。
| 実効線量係数 | 吸入 | 成人 | 2.6x10-10 Sv/Bq |
|---|---|---|---|
| 幼児 | 1.0x10-9 Sv/Bq | ||
| 摂取 | 成人 | 4.2x10-11 Sv/Bq | |
| 幼児 | 1.2x10-10 Sv/Bq | ||
| 排気中濃度限界(水素) | 70 Bq/cc | ||
| 排気中濃度限界(水蒸気) | 5x10-3 Bq/cc | ||
| 排気中濃度限界(メタン) | 7x10-1 Bq/cc | ||
| 排気中濃度限界(それ以外) | 3x10-3 Bq/cc | ||
| 排水中濃度限界(水) | 60 Bq/cc | ||
| 排水中濃度限界(メタン以外の有機化合物) | 20 Bq/cc | ||
| 排水中濃度限界(それ以外) | 40 Bq/cc | ||
図のように、トリチウムのβ線のエネルギーは、たった19keVしかありません。これまで紹介したどの放射線よりも小さなエネルギーです。そのため、人間が日常的に手で扱う多くのものを透過できず、かんたんに遮蔽されてしまいます。測定するときには、どんな測定器の外枠も透過することができないので、試料を液体状のシンチレーターの中に直接入れて測定するしかありません。
こんな弱弱しい放射性物質だけに、特に気をつける必要もないと思ってしまいがちです。測定もできないものなど、気にするな、と。ところが、これが水素の同位体であるということが、トリチウムをもっとも厄介な放射性同位体としているのです。水素は、その名のとおり、水の素だからです。
トリチウムが、水素分子の状態でいてくれたら、我々にとっては取るに足りない放射性同位体です。水素(分子)はきわめて水に溶けにくいので、人体には取り込まれにくいからです。水素水詐欺なんてものも流行ったことがありましたが、わざわざ水に溶けにくいものを選んでいるところが秀逸なジョークですよね。なぜああいう詐欺師たちは突っ込まれどころ満載のものをわざわざ選ぶのでしょうか。突っ込んでもらわないと話題にならないからでしょうか。
ところが、これが、別の化合物、水となったとたんに、トリチウムは厄介極まりない同位体となります。水はあらゆる生物の身体に含まれる物質であり、他のあらゆる物質を体内で循環させる溶媒だからです。水であれば、容易に体内に取り込まれますし、体内を存分に循環して、DNAのもっとも近くからこれを攻撃することも可能です。体内に取り込まれる場合を考えても、粉塵の吸入を防ぐことは容易ですが、水蒸気を防ぐことはかんたんではありません。
そしてより重要なことは、環境中から取り除くこともかんたんではない点です。第6章で水の中に溶けている放射性同位体を取り除く方法についてお話ししましたが、この方法でもトリチウムは取り除けません。なにせ、「水の中に溶けている」のではなく、「水そのもの」だからです。
みなさんの中にも、福島第一原子力発電所事故の処理で、汚染水がタンクに溜められているという話を聞いたことがあるかも知れません。あの「汚染」の正体は、トリチウムです。トリチウム以外のものは水の中から取り除けますから、そういうものはちゃんと取り除いて、そしてどうしても取り除けない「水そのもの」であるトリチウムが残ってしまった、というわけです。
事故がなくとも、トリチウムは原子炉の通常の運転で生成されます(一般的な沸騰水型原子炉の1年間の運転で20TBqていど)。このトリチウムは、どの国でも、通常は普通の水で希釈して、排水基準以下の濃度にしてから捨てています。水素1とトリチウムの同位体分離の方法もあるにはあるのですが(26)、とてもコストがかかるからです。
しかし、倫理的な問題もあり、コストを少しでも抑えながら分離する方法が模索されています。福島第一原子力発電所事故での汚染水処理では、ロシアの原子力企業であるРосатомの子会社であるРосРАОが、東京電力から依頼されて、トリチウム除去のプラントの開発を行いました。その試験がうまくいったとのプレスリリースが、2016年に出されています。これは、従来の同位体分離の方法を組み合わせることにより、コストダウンを実現したもののようです。РосРАОがつくった紹介映像もYoutubeに上がっています(27)。
しかし世の中には原子炉など比較にならないほど多くのトリチウムを環境に放出した人たちもいます。これまで何度か触れているとおり、国連の安全保障理事会の常任理事国です。彼らが大気内核実験により大気中に放出したトリチウムは、240,000,000,000,000,000,000 Bqにも及びます。これによって地球上のトリチウム量は大きく変わりました。そんなことをやらかした国連が、いまさら、したり顔で環境問題を取り上げられても、ねぇ…
捨てる神あらば拾う神ありで、トリチウムを積極的に使う場合もあります。たとえば核融合です。核融合炉でも、核融合兵器でも、デューテリウムとトリチウムとの反応(DT反応)
2H + 3H → 4He + n
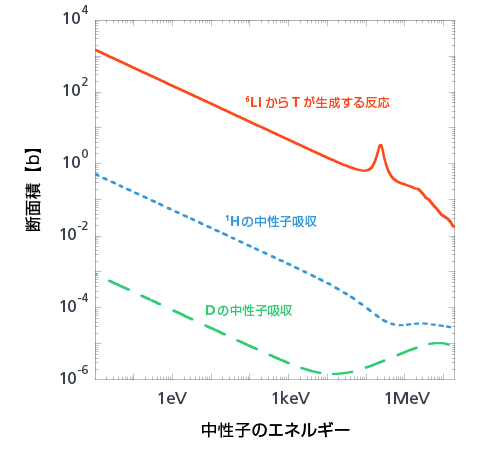
が、もっとも重要な反応です。デューテリウムは天然にあるていどの量が存在するのに対して、トリチウムはたとえ国連がせっせと大気中に放出したとしても、資源として利用できるほどの量はありませんから、人工的につくるしかありません。しかし水素に中性子を加えていく方法だと、さきほどお話ししたとおり、トリチウムだけ分離して取り出すのが大変です。そこで、リチウムと中性子との反応を使う方法があります。リチウムの同位体であるリチウム6(天然に存在します)は、中性子と反応して、
6Li + n → 4He + 3H
のようにトリチウムを生成します。この方法は、あとでトリチウムを分離しやすいだけでなく、中性子との反応断面積も大きいのが利点です(28)。そのため、核融合兵器では、その燃料として、デューテリウムとトリチウムを入れるのではなく、デューテリウムとリチウムの化合物である重水素化リチウムを入れます。
本来は、廃棄物となるトリチウムを回収して利用できれば、資源の有効活用という面ではとてもよいのですが、第7章でお話ししたとおり、放射線としての量と、我々がたとえば産業利用する物質としての量とには、大きく隔たりがあります。さきほどの原子炉で1年間につくられるトリチウムの量は、放射線で言えば20TBqと膨大な量ですが、これを比放射能(358TBq)で割って質量に換算すると、たったの0.6gにしかなりません。これでは核融合に使う量としてはまったくお話しにならないのです。
γ線を出す放射性同位体
γ線は、第2章でもお話ししたとおり、原子核のエネルギーが過剰にある場合に放出されるものです。ですから、本章でこれまで見てきた放射性同位体が、α線やβ線を出したあとに、まだエネルギーがあまっていて(図では紫色の原子核として表わしています)、γ線を出すような状態がこれに当たります。例として、セシウム137の図をもう一度載せておきます。
このとき、下の黒色のバリウム137は安定していてもう放射線を出しませんが、上の紫色のバリウム137はまだエネルギーがあまっている状態で、そのあまった分のエネルギーを出すことで安定して、下の状態になります。
このとき、α崩壊やβ崩壊のあとに直ちにγ線を出すのではなく、エネルギーが高い状態を少しの間保つ場合、この原子核を核異性体と呼びます。表記上は、バリウム137m(記号では137mBa)のように、mを添えて書きます。バリウム137mの場合は、この持続時間(半減期)が2.55分です。
そして、この持続時間ののちにγ線を出す反応を、特に、核異性体転移と呼びます。ここでは、ひとつだけ、この核異性体について取り上げておきましょう。
テクネチウム99m(99mTc)
テクネチウムは地球上にはほとんど存在せず、人工的につくる必要があります。人類が人工的につくった最初の元素です。なにせTechnetiumの語源がギリシア語で人工を意味するτεχνητόςです。そしてその同位体は全てが放射性です。
テクネチウムの同位体のうちもっとも重要なものはテクネチウム99mで、トレイサーとして、骨疾患、脳血管障害、甲状腺疾患、癌などの医療診断に広く使われています。医療診断に使われる放射性同位体としてはもっとも多く、利用件数は、世界で年間3,000万件、日本で年間100万件と言われています。
それぞれ測定したい部位に辿り着きやすいキレートの鋏にテクネチウム99mをはさんで、人体に投与します。
半減期がわずか6.01時間と短いことが、トレイサーとして選ばれた理由のひとつです。医療目的とは言え放射性物質を体内に投与するのですから、早くなくなるに越したことはありません。かと言って分単位のものでは、取り扱っている間になくなってしまいますので、この6時間というのがとてもいい感じなのです。
トレイサーとして選ばれたもうひとつの理由は、エネルギーが141keVと低いことです。
テクネチウム99mは、モリブデン99がβ崩壊してできます。
99Mo → 99mTc + e-(ニュートリノは省略)
テクネチウム99mは半減期がたった6時間しかないために、医療機関が直接製造所からそれを買ってきて使うことは現実的ではありません。仮に医療機関の隣のコンビニに売っていたとしても、コンビニに配送に来るトラック便は日に何度もありませんので、コンビニ弁当よりも日持ちしないテクネチウム99mを直接購入するのは現実的ではありません。しかも、その親のモリブデン99をつくっている場所は研究用原子炉で、世界に数か所しかありません。そんなレアな場所から運んで来なければならないのです。
そこで、テクネチウム99mを直接買うのではなく、その親のモリブデン99を購入し、それぞれの医療機関の中、もしくは医療機関の近くの国内にある製薬会社で、モリブデン99が崩壊によって随時生み出しているテクネチウム99mを抽出するのです。モリブデン99の半減期は65.9時間ですから、空輸すれば、途中であるていどは減るものの、なんとか使えます。日本でも、海外からの空輸が100%を占めています(29)。モリブデン99を扱っている日本の製薬会社は、日本メジフィジックスと富士フィルムRIファーマで、この両社が全国各地で運営している事業所から、テクネチウム99mを含むキレート剤や、モリブデン99の状態で、各医療機関に配達しています。
ところが、近年、その研究用原子炉が老朽化により運用を停止することが見込まれています。モリブデン99を供給している原子炉は、そのほとんどが50~60年代に運転を開始したもので、21世紀から運転を始めたのはわずか1基しかありません。そのため、これらの原子炉が廃炉になったあとにモリブデン99をどのようにして安定して供給するかが、喫緊の課題となっています。モリブデン99の需要は、これから増える一方だからです。
また、モリブデン99を製造する原子炉では、90%以上という高い濃縮度のウラン235を用い、その核分裂によって生成したモリブデン99を抽出しているのですが、この高濃縮ウランはまさに核兵器級であるため、単に技術的だけでなく社会的な問題もあります。
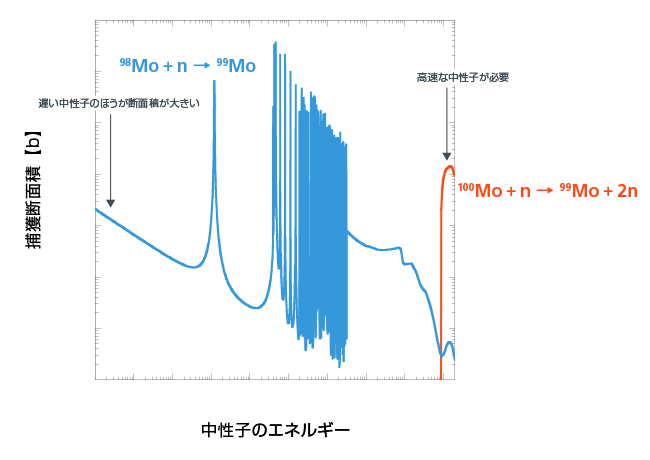
そこで、この従来の方法を改め、モリブデン98(安定した同位体で、天然のモリブデン中に最多の24%含まれる)に中性子を照射して中性子を捕獲させてつくる方法
98Mo + n → 99Mo
や、モリブデン100(同じく10%含まれる)に高速の中性子を照射して2つの中性子を叩き出してつくる方法
100Mo + n → 99Mo + 2n
などが研究されています(30)。後者の場合は、加速器を用いて高速の中性子を発生させます。
以上で、放射線についてのお話しは終わりです。いかがでしたでしょうか。最後にまとめを書いて、締めとさせて頂きます。
参照・注
- (1) 『アイソトープ手帳 第11版』、日本アイソトープ協会 (2011)
- (2) ICRP Publication 119
ここには、「摂取」に関して、体内での動きが異なる3つのモデルについてそれぞれ値が載っているのですが、このサイトでは、そのうち、最も大きな値を示すモデル(sモデル、slowモデル)を載せています。 - (3) 平成十二年科学技術庁告示第五号(放射線を放出する同位元素の数量等) 別表第1
- (4) 本来は、「壊変図式」という、崩壊の様子を表わした図があるのですが、一般の方は見慣れないと思い、このように新たにイラストを起こしてみました。余計にわかりにくくなってしまっていたとしたら、すみません。
- (5) 『The Nuclear Fuel Report』, World Nuclear Association
2015年の採掘量。 - (6) 『Uranium 2014 : Resources, Production and Demand』, OECD NEA & IAEA
2013年1月1日の時点。採掘単価がウラン換算1kg当たり130US$以下のもの。 - (7) かつて採掘が行われていた坑道は、現在公開されていますので、興味のある方は見学に行ってみるのもよいでしょう。
https://www.jaea.go.jp/04/zningyo/2-11.html - (8) http://www.who.int/mediacentre/factsheets/fs291/en/
- (9) 『Meta-analysis of residential exposure to radon gas and lung cancer』, Bulletin of the World Health Organization, 81, 732-738 (2003)
- (10) 『喫煙者の実効線量評価─タバコに含まれる自然起源放射性核種─』, RADIOISOTOPES, 59, 733-739 (2010)
- (11) 現在の核分裂兵器のイニシエイターには、デューテリウムとトリチウムの核融合反応を利用した中性子発生管が使われています。
- (12) 『Nuclear Safety Guide』, U.S. Nuclear Regulatory Commision, TID-7016 Revision 2 (1978)
- (13) 『Critical Parameters of Spherical Systems of Alpha-Phase Plutomium Reflected by Berillium』, University of California Radiation Laboratory Repot, UCRL-5349 (1958)
- (14) 『核兵器』に詳しく記述してありますので、そちらをごらんください! さきほどの中性子発生管についても載せてあります。
- (15) 『Investigation of the Chemical Explosion of Anion Exchange Resin Colum and Resulting Americium Contamination of Personel in the 242-Z Bulding』, Richland Operation Office (1976)
- (16) 『Spontaneous Fission Half-Lives for Ground-State Nuclides』, Pure and Applied Chemistry, 72, No.8, 1525 (2000) のデータより、著者が計算
- (17) JAEA Nuclear Data CenterのJENDL-4.0のデータより、著者がグラフ作成
- (18) セシウム137の生物学的半減期は、成人で110日ていど(ICRP Publication 30)、10歳児で50日ていど(ICRP Publication 67)です。
- (19) 反応のしやすさを表わす値は、「断面積」と呼び、面積の次元をもちます。ここで登場している「b(バーン)」は、
1b = 10-28m2です。 - (20) JAEA Nuclear Data Center
- (21) http://www.gasukai.co.jp/gas/index4.html
- (22) 『Sources and Effects of Ionizing Radiation』, United Nations Scientific Committee on the Effects of Atomic Radiation (2011)
- (23) 以下、この段落は、『人体内放射能の除去技術』、講談社 (1996) より。
- (24) かつては乳癌の治療にコバルト60によるγ線照射がさかんに行われていましたが、粒子線治療が普及してからは随分減ってきています。
- (25) 『メキシコ-米国における治療用60Co線源紛失事故顛末記』, 放射線科学, 28, 268 (1985)
- (26) トリチウムの同位体分離には、蒸留法、同位体交換法、電気分解法などがあります。詳しくは、https://fukushima.jaea.go.jp/initiatives/cat05/pdf/20140311.pdf [PDF] などをごらんください。
- (27) このプラントの紹介映像は、https://www.youtube.com/watch?v=pPOBAZswT9Q でごらんいただけます。
- (28) 水素1がトリチウムになるには、まず水素1が中性子を吸収してデューテリウムとなり、そのデューテリウムが中性子を吸収してトリチウムになる過程を経ます。ところが、デューテリウムは中性子を吸収しにくいのです。水素1とデューテリウムが中性子を吸収(捕獲)する反応の断面積と、リチウム6が中性子を吸収してトリチウムを生成する反応の断面積を比較すると、 となります。リチウム6からトリチウムを生成する反応のほうが、けた違いに起こりやすいことがわかります。
- (29) 日本に輸入する場合の典型的な日数は、原子炉に元になる核燃料(ウラン235)を入れておくのが4~10日、そこから取り出した使用済み核燃料からモリブデン99を抽出するのに1~2日、航空輸送に2日、製薬会社で投与できる状態にして医療機関に届けるのが2~3日、といったところです。日本は主にカナダから購入していますが、南アフリカでも製造しているので、そこから買う場合、空輸時間が長くなるために量が減ってしまう、などという、数時間の時間差が問題となるような世界です。まさに時間との勝負、といった感じです。
- (30) モリブデン98が中性子を捕獲する反応と、モリブデン100に1つの中性子を衝突させて2つの中性子を叩き出す反応との断面積は、 となります。前者の反応では遅い中性子のほうが反応断面積が大きいのですが、後者の反応を起こすためには、十数MeV附近の高速の(エネルギーが大きい)中性子が必要であることがわかります。
※通常、引用論文は、「著者名、雑誌名、巻数、ページ数、年」、の順で書きますが、本サイトでは、みなさんがぐぐりやすいよう、著者名の代わりにタイトルを書いてあります
著者プロフィール
多田将 (ただ・しょう)
京都大学理学研究科博士課程修了、理学博士。
高エネルギー加速器研究機構 素粒子原子核研究所 准教授。
著書に『すごい実験』『すごい宇宙講義』(以上、中公文庫)『宇宙のはじまり』『ミリタリーテクノロジーの物理学<核兵器>』『ニュートリノ』(以上イースト・プレス)『放射線について考えよう。』『核兵器』『兵器の科学1 弾道弾』(以上、明幸堂)『ソヴィエト連邦の超兵器 戦略兵器編』(ホビージャパン)がある。